رویکردهای فارماکولوژیک در درمان دیابت، استانداردهای مراقبت پزشکی در دیابت 2021

رویکردهای فارماکولوژیک در درمان دیابت، استانداردهای مراقبت پزشکی در دیابت 2021، گاید لاین انجمن دیابت آمریکا ۲۰۲۱
رویکردهای فارماکولوژیک در درمان دیابت، استانداردهای مراقبت پزشکی در دیابت 2021، گاید لاین انجمن دیابت آمریکا ۲۰۲۱
درمان دارویی برای دیابت نوع 1
توصیه ها
اکثر افراد مبتلا به دیابت نوع ۱ باید با تزریق روزانه چندین نوبت از انواع انسولین شامل یک دز انسولین پایه و ۳ نوبت انسولین قبل وعده های غذایی (MDI) و یا تزریق مداوم انسولین زیر جلدی توسط پمپ ( pump therapy) تحت درمان قرار گیرند.
اکثر افراد مبتلا به دیابت نوع ۱ برای کاهش خطر افت قند خون ( هیپوگلیسمی ) باید از انسولین سریع اثر آنالوگ استفاده کنند.
بیماران مبتلا به دیابت نوع ۱ باید در مورد چگونگی مطابقت دوزهای انسولین قبل غذا با مقدار کربوهیدرات موجود در غذا ، گلوکز قبل از غذا و میزامفعالیت بدنی آموزش ببینند.
انسولین درمانی ( insulin therapy )
از آنجا که مشخصه اصلی دیابت نوع ۱ اختلال شدید در عملکرد سلول β و یا از بین رفتن کامل فعالیت آن است بنابر این در بدن مبتلایان تقریباً انسولین به طور طبیعی وجود ندارد و تجویز انسولین ضروری است. علاوه بر افزایش قند خون ، عدم وجود انسولین می تواند منجر به سایر اختلالات متابولیکی مانند افزایش چربی های خون ( هیپرتری گلایسیریدمی) و کتواسیدوز و همچنین کاتابولیسم بافت های بدن و تهدید زندگی باشد. در طی شش یا هفت دهه پس از کشف انسولین ، با استفاده از تزریق یک و یا دوبار انسولین از بوجود آمدن این عوارض جلوگیری می شد. . با این وجود ، طی سه دهه گذشته ، با جمع آوری شواهد نشان داده شد که جایگزینی شدید انسولین با استفاده از چندین تزریق روزانه و یا تجویز زیر جلدی مداوم از طریق پمپ انسولین ، بهترین و مطمئن ترین راه برای درمان مبتلایان به دیابت نوع ۱ است. نتایج مطالعه ی DCCT نشان داد که درمان شدید با تزریق چند دز روزانه و یا تزریق مداوم زیر جلدی انسولین (CSII) A1C را کاهش می دهد و با بهبود نتایج طولانی مدت همراه است. این مطالعه با انسولین های انسانی کوتاه اثر (رگولار) و متوسط اثر (NPH) انجام شد. بر اساس نتایج این مطالعه ی مهم ، A1C پایین تر با کنترل شدید (7٪) (intensive control) منجر به کاهش 50٪ در عوارض میکرو واسکولار در طی 6 سال درمان شد. با این حال ، درمان شدید با میزان بالاتر کاهش شدید قند خون ( هیپوگلیسمی ) نسبت به درمان معمولی همراه بود (62 در مقایسه با 19 مورد در هر 100 بیمار در یک سال درمان). پیگیری افراد مورد مطالعه ی DCCT برای بیش ۱۰ سال پس از پایان پروژه نشان داد افرادی که تحت درمان شدید قرار داشته اند به مراتب کمتر دچار عوارض ماکرو واسکولار و میکروواسکولار شده اند.
در طول ۲۵ سال گذشته ، انسولین های آنالوگ کوتاه اثر و طولانی اثر پا به عرصه ی ظهور نهاده اند که دارای اثرات فارماکوکینتیک و فارماکو دینامیک متفاوت با انسولین های انسانی قبلی هستند. انسولین های آنالوگ پایه (basal ) دارای مدت زمان طولانی تری با غلظت پلاسما یی ثابت تر نسبت به انسولین NPH هستند. آنالوگهای سریع اثر (RAA) نسبت به انسولین انسانی معمولی ( regular) داری شروع اثر و اوج سریع تر و مدت زمان کوتاهتر هستند. در افراد مبتلا به دیابت نوع 1 ، استفاده از انسولین های آنالوگ باعث کاهش شدید کمتر قند خون ( هیپوگلیسمی ) ، افزایش وزن کمتر و همچنین A1C پایین تر در مقایسه با انسولین های انسان می شود. اخیراً ، دو فرمول جدید انسولین با پروفیل های عمل سریع تر معرفی شده است. انسولین انسانی استنشاقی در مقایسه با RAA دارای اوج سریع تر و مدت زمان اثر کوتاه تری است و ممکن است باعث کاهش کمتر در بروز هیپوگلیسمی و افزایش وزن کمتری شود .انسولین آسپارت انسولین با اثر سریعتر faster acting insulin aspart و انسولین لیسپرو سریع اثر ( lipro-aabc ) ممکن است در کنترل افزایش قند بعد غذا بهتر از RAA عمل کنند. برای روشن میزان اثر این نوع انسولین ها در درمان و مدیریت دیابت به تحقیقات بیشتری نیاز است. علاوه بر این ، آنالوگهای جدید با عملکرد طولانی تر (U-300 گلارژین یا دگلودک degludec) ممکن است در مقایسه با U-100 گلارژین در بیماران مبتلا به دیابت نوع ۱ هیپوگلیسمی کمتری ایجاد کنند. با وجود مزایای انسولین های آنالوگ در درمان مبتلایان به دیابت نوع ۱ ، ممکن است قیمت و هزینه های این انسولین ها موانعی برای مصرف آنها در بعضی از بیماران ایجاد کند. رویکردهای متعددی برای درمان با انسولین وجود دارد ولی هدف تمام آنها کنترل قند خون با حداقل بروز هیپوگلیسمی، جلوگیری از بروز کت و اسیدوز، جلوگیری از بوجود آمدن عوارض و کنترل قند خون در حد امکان در محدوده ی طبیعی است.
بیشتر مطالعات برای مقایسه ی چندین تزریق روزانه (MDI) با درمان با پمپ (CSII ) نسبتاً کوچک و با مدت زمان کوتاه بوده اند. با این حال ، یک بررسی سیستماتیک و متاآنالیز اخیر به این نتیجه رسیده است که پمپ درمانی دارای مزایای متوسطی در مقایسه با MDI برای کاهش A1C (.0.30) و کاهش میزان شدید افت قند خون در کودکان و بزرگسالان است . با این حال ، هیچ اتفاق نظری برای انتخاب تزریق یا پمپ درمانی در یک بیمار معین وجود ندارد و تحقیقات بیشتری برای رسیدن به تصمیم گیری صحیح لازم است. تاثیرات مثبت مانیتورهای مداوم گلوکز در مدیریت قند خون Glucose monitoring system در بسیاری از موارد به اثبات رسیده است. استفاده از سنسورهای گلوکز با قطع خودکار انسولین در بیمارانی که از CSII استفاده می کنند می تواند منجر به کاهش هیپوگلیسمی شبانه شود. هنگام انتخاب از بین روش های مختلف انسولین درمانی باید مواردی مانند ترجیح بیمار ، هزینه و نوع انسولین مصرفی نظر گرفته شود.
سازمان غذا و داروی ایالات متحده (FDA) اکنون دو سیستم پمپ حلقه بسته ترکیبی ( hybrid closed-loop pump systems)را تأیید کرده است. ایمنی و کارآیی این سیستم ها در نوجوانان و بزرگسالان مبتلا به دیابت نوع 1 نشان داده شده است. و شواهد اخیر نشان می دهد که hybrid closed-loop pump systems در مقایسه با ترکیب پمپ همراه با سنسور در کنترل قند خون و کاهش هیپوگلیسمی در یک دوره ی ۳ ماهه در کودکان و بزرگسالان مبتلا به دیابت نوع 1 مفید تر بوده است. در مطالعه ی International Diabetes Closed Loop (iDCL) ، در یک دوره ی 6 ماهه در بیماران دیابتی نوع 1 با سن حداقل ۱۴ سال، استفاده از closed loop در مقایسه با پمپ درصد بیشتری از بیماران در میزان قند خون تعیین شده ی هدف بوده اند ، متوسط قند خون و A1C پایین تری داشته اند و مدت زمان کمتری در هیپوگلیسمی بوده اند.
درمان شدید دیابت با استفاده از پمپ و پایش مداوم قند خون در بیشتر بیماران نوع ۱ دیابت باید در نظر گرفته شود. سیستمهای تزریق خودکار انسولین ممکن است در بزرگسالان مبتلا به دیابت نوع 1 که مهارت لازم برای استفاده از آنها را دارند به منظور دستیابی به بیشترین زمان نگه داشتن قند خون در محدوده ی طبیعی، کاهش A1C و هیپوگلیسمی کمتر مد نظر قرار گیرند.
به طور کلی ، بیماران مبتلا به دیابت نوع 1 به ۵۰٪ انسولین روزانه به عنوان پایه و ۵۰٪ به صورت قبل از وعده های غذایی نیاز دارند. کل نیاز روزانه به انسولین را می توان بر اساس وزن تخمین زد. نیاز روزانه ی این بیماران حدود ۴/ تا ۱ واحد به ازای هر کیلو گرم وزن است. به مقادیر بیشتری در دوران بلوغ ، بارداری و بیماری ها نیاز است. انجمن دیابت آمریکا دز ۰/۵ واحد به ازای هر کیلو گرم وزن بدن را در بیمارانی که از نظر متابولیک در شرایط پایدار هستند پیش نهاد می کند. نیمی از آن به عنوان انسولین پایه برای کنترل قند خون در بین وعده های غذایی و نیم دیگر به عنوان انسولین قبل غذا برای کنترل قند بعد از غذا تجویز می شود.
در رژیم های چند وعده ای معمولی برای بیماران مبتلا به دیابت نوع 1 ، انسولین های کوتاه اثر را قبل از وعده های غذای و انسولین پایه را غالبا در شب تزریق می کنند. زمان مناسب برای تجویز انسولین قبل غذا ، بر اساس فارماکوکینتیک فرمولاسیون ( رگولار ، RAA ، استنشاقی) ، سطح گلوکز قبل از غذا و مصرف کربوهیدرات متفاوت است. ترشح انسولین فیزیولوژیک با میزان قند خون ، اندازه وعده غذایی و نیازهای بافتی به گلوکز متفاوت است. بنابراین ، آموزش به بیماران در مورد چگونگی تنظیم انسولین قبل غذا با در نظر گرفتن مصرف کربوهیدرات ، سطح گلوکز قبل از غذا و فعالیت پیش بینی شده می تواند موثر باشد و باید به اکثر بیماران ارائه شود. برای افرادی که از شمارش کربوهیدرات استفاده می کنند ، تخمین میزان چربی و پروتئین وعده های غذایی را می توان در دوز اصلی آنها برای سود بیشتر وارد کرد.
روش تزریق انسولین
اطمینان از درک صحیح روش تزریق انسولین توسط بیماران و یا مراقبان ، برای بهبود کنترل قند خون بسیار مهم است. بنابراین مهم است که انسولین به روش صحیح به داخل بافت مناسب تزریق شود. منابع زیادی برای فرا گیری روش تزریق انسولین در دسترس است. نکات مهم در تزریق مناسب انسولین عبارتند از تزریق به مناطق مناسب بدن ، چرخش محل تزریق ، مراقبت های مناسب از محل های تزریق برای جلوگیری از عفونت یا عوارض دیگر و جلوگیری از تزریق انسولین به روش عضلانی است.
انسولین باید در بافت زیرپوستی تزریق شود و در داخل عضله تزریق نشود. محل های توصیه شده برای تزریق انسولین عبارتند از شکم ، ران ، باسن و بالای بازو . از آنجا که جذب انسولین در تزریق عضلانی با توجه به فعالیت عضله متفاوت است ممکن است منجر به نتایج غیرقابل پیش بینی و هیپوگلیسمی مکرر در سطح قند خون شود. خطر تزریق انسولین عضلانی در کودکان و افراد لاغر در هنگام تزریق به اندام ها به جای تنه (شکم و باسن) و استفاده از سوزن های بلند به مراتب بالاتر است. شواهد اخیر نشان داده است که استفاده از سوزن های کوتاه (به عنوان مثال ، سوزن های قلم 4 میلی متری) در مقایسه با سوزن های بلند تر ، به عنوان روشی موثر و قابل اعتماد در تزریق انسولین حتی در افراد چاق مفید هستند.
چرخش محل تزریق می تواند از لیپوهیپرتروفی بافت چربی که به علت اثر چربی زایی ( لیپوژنسیتی ) انسولین به علت تزریق مکرر در یک محل است ، جلوگیری کند. لیپوهیپرتروفی به صورت نواحی منظم و نرم چند سانتی متری ظاهر می شود و می تواند باعث جذب نامنظم انسولین و در نتیجه نتایج غیر قابل پیش بینی در سطح قند خون شود. بیماران و یا مراقبان آنها باید در مورد اهمیت تزریق چرخشی در تنظیم و کنترل قند خون آموزش های لازم را ببینند. بیماران باید در هر مراجعه از نظر محل تزریق انسولین و وجود و یا عدم وجود هیپرتروفی مورد معاینه قرار بگیرند ، وسیله ی تزریق آنها مانند سرنگ و یا قلم مورد بازدید واقع شود و در مورد استفاده ی صحیح آن ارزیابی شوند .
درمان های غیر انسولین برای دیابت نوع 1
اثر بخشی داروهای تزریقی و خوراکی مختلف به عنوان مکمل های درمان انسولین برای دیابت نوع 1 مورد مطالعه قرار گرفته اند
پراملینتید ( pramlintide) : بک آنالوگ هورمون آمیلین ( amylin) است که به طور طبیعی از سلولهای بتا پانکراس ترشح می شود. ابن دارد برای استفاده در بزرگسالان مبتلا به دیابت نوع 1 مورد تایید FDA قرار گرفته است. نتایج حاصل از مطالعات کنترل شده تصادفی ( RCT) ، نشان داده است که افزودن این دارو به انسولین باعث کاهش A1C (بین ۰ تا ۳/ درصد) و کاهش وزن بدن (1–2 کیلوگرم) می شود.
متفورمین: افزودن متفورمین در بزرگسالان مبتلا به دیابت نوع ۱ باعث کاهش اندکی در وزن بدن و سطح چربی های خون می شود اما تاثیری در بهبود A1C ندارد.
آنالوگ های GLP-1 :افزودن این داروها مانند لیراگلوتید ( Liraglutide )یا اگزناتید ( Exenetide) به انسولین درمانی باعث کاهش اندکی در A1C ( به میزان ۲/ درصد ) در مقایسه با انسولین به تنهایی در افراد مبتلا به دیابت نوع ۱ و همچنین کاهش وزن بدن ( حدود ۳ کیلوگرم ) می شوند.
مهار کننده های SGLT-2
افزودن این داروها به انسولین باعث بهبود A1C و کاهش وزن بدن در مقایسه با انسولین به تنهایی می شوند . با این حال ، استفاده از مهار کننده های SGLT2 در دیابت نوع ۱ با افزایش دو تا چهار برابر کتواسیدوز همراه است. به خاطر داشته باشید فقط پراملینتاید برای درمان دیابت نوع ۱ تأیید می شود.
درمان جراحی برای دیابت نوع ۱
پیوند لوزالمعده و جزایر
پیوند موفقیت آمیز پانکراس و یا جزایر بتا می تواند باعث عادی شدن قند خون شود و عوارض عروقی دیابت نوع ۱ را کاهش دهد. با این حال ، بیمارانی که از این روش های درمانی استفاده می کنند برای جلوگیری از رد پیوند و یا عود تخریب جزایر بتا ی خود ملزم به استفاده از داروهای سرکوبگر سیستم ایمنی به صورت مادام العمر هستند. با توجه به عوارض جانبی بالقوه درمان سرکوب سیستم ایمنی ، پیوند پانکراس فقط باید برای بیماران مبتلا به دیابت نوع ۱ که به طور همزمان نیاز به پیوند کلیه دارند و یا قبلا مورد پیوند کلیه قرار گرفته اند مد نظر قرار گیرد. همچنین در بیمارانی که کتواسیدوز مکرر دارند و یا افت مکرر و شدید قند خون دارند نیز کمک کننده است.
درمان دارویی برای دیابت نوع ۲
توصیه ها
۱- متفورمین داروی اولیه و ترجیحی برای درمان دیابت نوع ۲ است.
۲- متفورمین پس از شروع ، باید تا زمانی که تحمل شود و منع مصرف نداشته باشد ، ادامه یابد. سایر عوامل ، از جمله انسولین ، باید به متفورمین اضافه شوند.
۳- درمان ترکیبی چند دارویی اولیه می تواند در برخی از بیماران هنگام شروع درمان در نظر گرفته شود تا شکست درمان کاهش یابد.
۴- در صورت شواهدی مبنی بر کاتابولیسم مداوم (کاهش وزن) و یا علائم هیپرگلیسمی شدید و یا مقدار A1C بیش از ۱۰ درصد و یا مقدار قند خون بیش یا مساوی ۳۰۰ میلی گرم در دسی لیتر ، شروع انسولین به عنوان اولین خط درمان باید مورد توجه قرار گیرد.
۵- در انتخاب عوامل دارویی باید از رویكرد بیمار محور استفاده شود. ملاحظاتی مانند تأثیر دارو روی بیماریهای قلبی عروقی و کلیوی ، میزان اثربخشی ، خطر افت قند خون ، تأثیر بر وزن ، هزینه ، خطر ابتلا به عوارض جانبی و ترجیح بیمار در انتخاب نوع دارو باید مد نظر قرار گیرند.
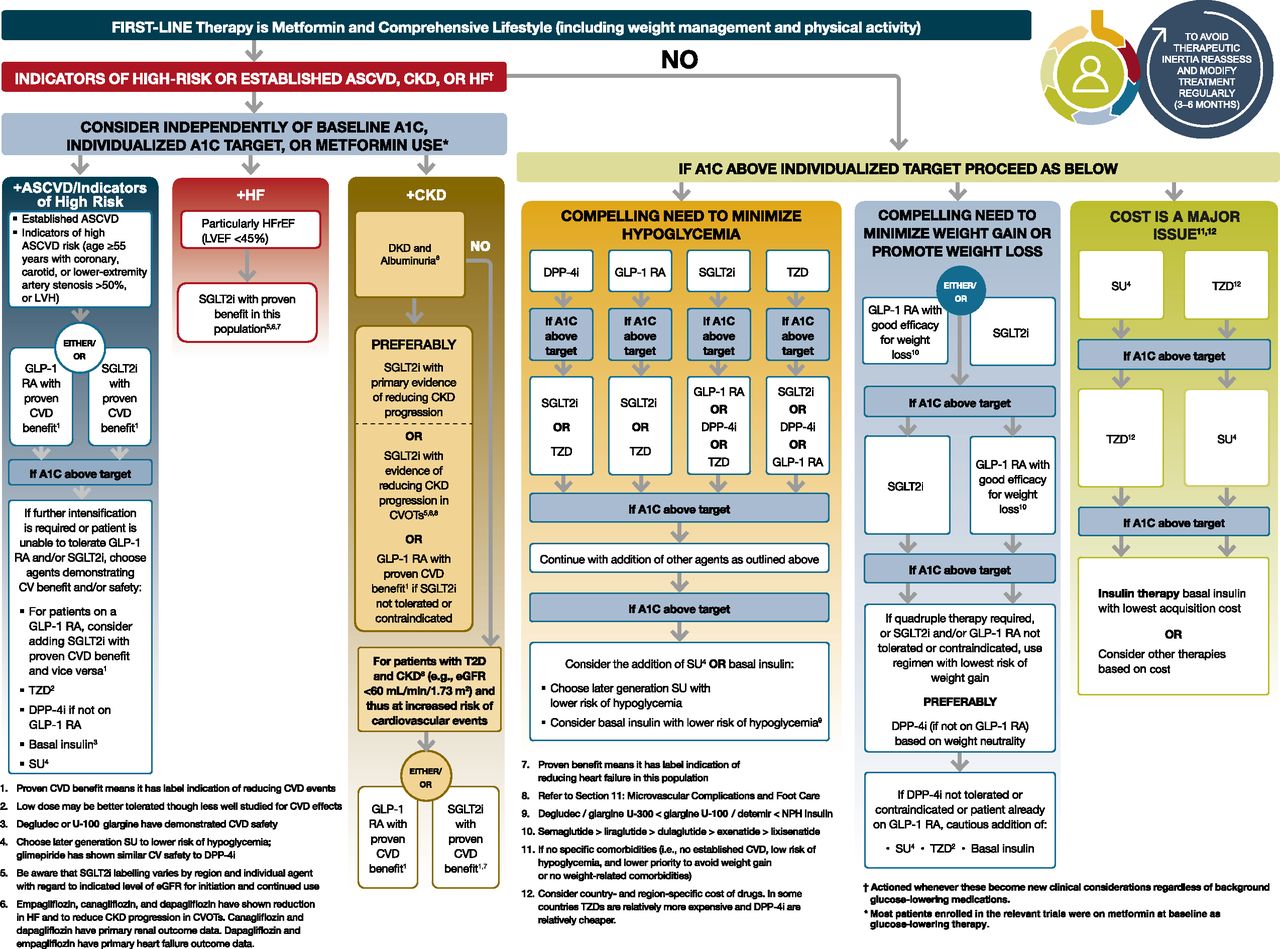
۶- بیماران مبتلا به دیابت نوع ۲ که بیماری قلبی عروقی آترواسکلروتیک (ASCVD) دارند یا شاخص های خطر بالا دارند و یا بیماری کلیوی یا نارسایی قلبی دارند ، یک مهار کننده گیرنده ی پمپ سدیم-گلوکز کوتراسپانسر ۲ (SGLT2 inhibitors ) و یا آگونیست های گیرنده پپتید ۱ (GLP-1 analogue ) با مزایای بیماری قلبی عروقی ثابت شده، به عنوان بخشی از رژیم دارویی کنترل قند خون مستقل از A1C و با در نظر گرفتن فاکتورهای خاص باید مد نظر قرار گیرند.
۷- در بیماران دیابتی نوع ۲ ، آگونیست گیرنده پپتید ۱ ( GLP-1 analogue) ، در صورت امکان به انسولین ترجیح داده می شود.
۸- تشدید درمان برای بیمارانی که به اهداف درمانی توصیه شده نمی رسند نباید به تأخیر بیفتد.
۹- رژیم دارویی و نحوه ی مصرف دارو باید در فواصل منظم (هر ۳ تا ۶ ماه یک بار) ارزیابی مجدد شود و در صورت لزوم تغییرات لازم انجام شود.
۱۰- پزشکان باید از خطرات استفاده ی بیش از حد از انسولین پایه (overbasalization) آگاهی داشته باشند. نشانه های استفاده ی بیش از مقدار انسولین پایه عبارتند از مصرف بیش از ۵/ ( نیم واحد) انسولین پایه به ازای هر کیلوگرم وزن بدن، تفاوت زیاد بین مقدار قند خون قبل خواب و صبح ناشتا، تفاوت زیاد بین قند خون قبل و بعد از غذا و افت های مکرر قند خون ( با آگاهی و یا بدون آگاهی ) در شبانه روز. در صورت وجود موارد بالا نوع درمان بیمار باید مورد ارزیابی مجدد قرار بگیرد.
درمان اولیه
متفورمین باید در زمان تشخیص دیابت نوع ۲ به عنوان اولین دارو شروع شود مگر اینکه موارد منع مصرف وجود داشته باشد. برای بسیاری از بیماران ، این درمان مونوتراپی در ترکیب با اصلاح سبک زندگی موثر خواهد بود. داروهای اضافی و یا جایگزین ممکن است در شرایط خاص در نظر گرفته شوند ، مانند افرادی که بیماریهای قلبی عروقی و یا کلیوی دارند. متفورمین موثر و بی خطر و ارزان است و ممکن است خطر حوادث قلبی عروقی و مرگ را کاهش دهد. متفورمین به دو صورت جذب فوری برای دوز دو بار در روز و فرم آهسته رهش که می تواند یک بار در روز تجویز شود در دسترس است. در مقایسه با سولفونیل اوره ، متفورمین به عنوان درمان خط اول اثرات مفیدی بر A1C ، وزن و مرگ و میر قلبی عروقی دارد. شواهد سیستماتیک کمی برای سایر داروهای خوراکی به عنوان درمان اولیه دیابت نوع ۲ در دسترس است.
عوارض اصلی متفورمین عبارتند از نفخ ، ناراحتی شکمی و اسهال. این موارد را می توان با کاهش دوز و افزایش تدریجی آن از بین برد. این دارو با فیلتراسیون از کلیه دفع می شود بنابر این در مواردی مانند کاهش حجم و یا فشار خون و یا نارسایی کلیه ها می تواند در بدن انباشت شود و منجر به لاکتیک اسیدوز شود. با این حال ، احتمال وقوع این عارضه بسیار نادر است . FDA برچسب متفورمین را اصلاح کرده است و استفاده از آن را در بیمارانی که eGFR بیش و یا مساوی ۳۰ میلی لیتر در دقیقه به ازای ۱/۷۳ متر مربع سطح بدن دارند مجاز شمرده است. یکمطالعه ی RCT مشاهدات قبلی در مورد وقوع کمبود ویتامین B12 در بیمارانی که از متفورمین استفاده می کنند را تایید کرده است. استفاده از متفورمین با کمبود ویتامین B12 و بدتر شدن علائم نوروپاتی مرتبط است. این یافته ها با گزارشی از مطالعه نتایج پیشگیری از دیابت (DPPOS) سازگار است که آزمایش دوره ای ویتامین B12 را پیشنهاد می کند.
در بیماران با موارد منع مصرف یا عدم تحمل متفورمین ، درمان اولیه باید بر اساس عوامل بیمار محور باشد. دارویی را از کلاس دیگری که در شکل 9.1 نشان داده شده در نظر بگیرید. وقتی A1C بیش یا مساوی ۱/۵٪ از اهداف درمانی بالاتر باشد در اغلب بیماران به دو دارو به عنوان شروع درمان برای رسیدن به اهداف درمانی نیاز است. انسولین این مزیت را دارد که در مواردی که داروهای دیگر در کنترل قند خون موثر نیستند موثر است . در موارد افزایش شدید قند خون انسولین باید جزئی از هر نوع ترکیب دارویی باشد. خصوصاً اگر ویژگی های کاتابولیک (کاهش وزن ، هیپرتری گلیسیریدمی ، کتوز) وجود داشته باشد. در بیمارانی که با قند خون برابر و یا بیش از ۳۰۰ میلی گرم در دسی لیتر دارند و یا A1C بیش از ۱۰٪ است و یا علایم افزایش شدید قند خون مانند پر نوشی و پر ادراری وجود دارد و یا شواهدی برای کاتابولیسم و شکیت بافت های بدن مانند کاهش وزن وجود دارد به عنوان خط اوا درمان باید مورد استفاده قرار بگیرد. در اغلب موارد با برطرف شدن مسمومیت گلوکز تغییر به روشهای ساده تر درمان مانند تغییر به داروهای خوراکی امکان پذیر است. با این حال ، شواهدی وجود دارد که بیماران مبتلا به هایپرگلیسمی کنترل نشده همراه با دیابت نوع ۲ را می توان به طور موثر با سولفونیل اوره نیز درمان کرد.
ترکیبی درمانی
از آنجا که دیابت نوع ۲ در بسیاری از بیماران یک بیماری پیشرونده است ، حفظ اهداف قند خون با مونوتراپی در اغلب موارد فقط برای چند سال امکان پذیر است و پس از آن درمان ترکیبی لازم می شود. بر اساس توصیه های فعلی داروها را باید به صورت مرحله ای به متفورمین برای حفظ A1C در محدوده ی هدف افزود. . این روش امکان ارزیابی واضحتر از تأثیرات مثبت و منفی داروهای جدید را فراهم می کند و خطر و هزینه بیمار را کاهش می دهد. بر اساس این عوامل ، افزودن متوالی عوامل خوراکی به متفورمین استاندارد مراقبت بوده است. با این حال شواهدی وجود دارد که نشان می دهد استفاده از داروهای ترکیبی از همان ابتدا ممکن است رسیدن به اهداف درمانی را سریعتر و مدت زمان کنترل قند خون را طولانی تر کند. بر اساس مطالعه ی VERIFY (اثر Vildagliptin در ترکیب با metformin برای درمان اولیه دیابت نوع ۲) نشان داده است که درمان ترکیبی اولیه نسبت به افزودن متوالی داروها در رسیدن سریع تر به اهداف درمانی و افزایش طول مدت کنترل قند خون ارجحیت داشته است. بر اساس مطالعه ی VERIFY ، شرکت کنندگانی که ترکیب اولیه متفورمین و مهارکننده دیپپتیدیل پپتیداز ۴ (DPP-4) ویلداگلیپتین را دریافت می کردند ، کاهش کنترل قند خون در مقایسه با متفورمین به تنهایی و ویلداگلیپتین که به ترتیب به متفورمین اضافه می شود ، کاهش کندتری در مدت کنترل قند خون دارند. این نتایج را نمی توان به غیر از ویلداگلیپتین به داروهای خوراکی دیگر تعمیم داده ، اما نشان می دهند که درمان زودرس شدیدتر فوایدی دارد و باید در صورت لزوم از طریق یک فرآیند تصمیم گیری مشترک با بیماران در نظر گرفته شود. علاوه بر این ، از آنجا که اثربخشی مطلق اکثر داروهای خوراکی به ندرت از ۱٪ فراتر می رود ، درمان ترکیبی اولیه باید در بیمارانی که دارای سطح A1C برابر یا بیش از ۱/۵ تا ۲٪ بالاتر از هدف هستند ، در نظر گرفته شود.
روش های تشدید درمان برای بیمارانی که اهداف درمانی را برآورده نمی کنند نباید به تأخیر بیفتد. تصمیم گیری مشترک در بحث های مربوط به تشدید درمان مهم است. انتخاب دارویی که به متفورمین اضافه می شود براساس مشخصات بالینی بیمار و ترجیحات وی است. از ویژگی های مهم بالینی می توان به وجود ASCVD یا شاخص های مشخص شده در مورد خطر بالای ASCVD ، نارسایی قلبی ، CKD ، سایر بیماری های همراه و خطر برای اثرات جانبی دارویی خاص و همچنین ایمنی ، تحمل و هزینه اشاره کرد. اگرچه مطالعات متعددی وجود دارد که درمان دوگانه را فقط با متفورمین مقایسه می کند ، اما شواهد کمی وجود دارد که بتواند ترکیبی را با ترکیب دیگر مقایسه کند. یک متاآنالیز اثربخشی مقایسه ای نشان می دهد که هر گروه جدید از داروهای غیر انسولینی که به درمان اولیه با متفورمین اضافه می شوند ، A1C را تقریباً ۰/۷ تا ۱٪ کاهش می دهد. اگر هدف A1C تقریباً بعد از ۳ ماه محقق نشود ، متفورمین را می توان با هر یک از شش گزینه درمانی ترکیب کرد: سولفونیل اوره ، تیازولیدیندیون ، مهار کننده DPP-4 ، آنالوگ های جی ال پی 1 - GLP ، مهار کننده SGLT2 یا انسولین پایه. برای انتخاب نوع دارو باید مشخصات دارو و بیمار را در نظر گرفت.
برای بیماران مبتلا به ASCVD یا شاخص های خطرناک بالا برای ASCVD (مانند بیماران با سن بیش یا برابر ۵۵ سال مبتلا به تنگی عروق کرونر ، کاروتید یا شریان اندام تحتانی به میزان بیش از ۵۰ ٪ یا هیپرتروفی بطن چپ) ، نارسایی قلبی یا CKD ، آنالوگ های جی ال پی 1 - GLP و مهار کننده SGLT2 با اثرات مفید ثابت شده مستقل از استفاده از متفورمین و یا میزان A1C توصیه می شود. برای بیمارانی که ASCVD آنها مشخص نیست ، شاخص های خطر بالای ASCVD ، نارسایی قلبی یا CKD ندارند انتخاب عامل دوم برای افزودن به متفورمین هنوز توسط شواهد تجربی مقایسه نشده است و انتخاب دارو براساس اثربخشی ، جلوگیری از عوارض جانبی (به ویژه کاهش قند خون و افزایش وزن) ، هزینه و ترجیحات بیمار است. ملاحظات مشابه در بیمارانی که برای رسیدن به اهداف قند خون به عامل سوم نیاز دارند ، اعمال می شود. یک بررسی سیستماتیک و متاآنالیز نشان می دهد بیشترین کاهش در سطح A1C مربوط به رژیم های است که انسولین و یا انالوگ های GLP-1 به متفورمین اضافه می شوند. در همه موارد ، رژیم های درمانی باید به طور مداوم از نظر اثر بخشی ، عوارض جانبی و هزینه برای بیمار بررسی شوند. در برخی موارد ، بیماران نیاز به کاهش یا قطع دارو دارند. دلایل رایج این امر عبارتند از: عدم تأثیر ، عوارض جانبی غیر قابل تحمل ، هزینه یا تغییر در اهداف درمانی.
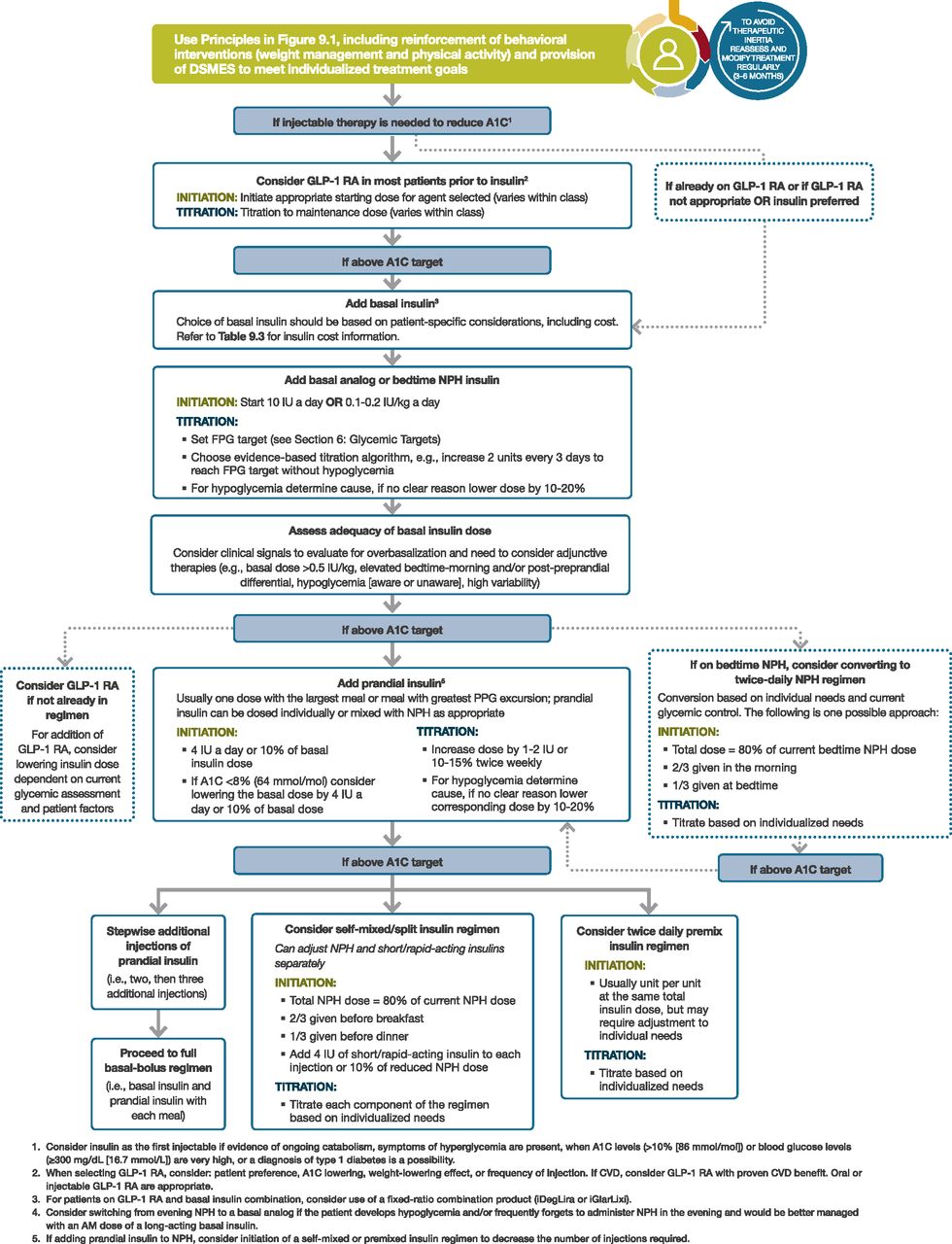
نیاز به افزودن داروهای تزریقی ، به ویژه در افرادی که مدت بیشتری دیابت دارند ، معمول است. افزودن انسولین پایه ، NPH انسانی و یا یکی از آنالوگهای انسولین با اثر طولانی مدت ، به رژیمهای خوراکی یک رویکرد کاملاً ثابت در درمان دیابت است که برای بسیاری از بیماران موثر است. علاوه بر این ، شواهد اخیر قابلیت استفاده از GLP-1 RA در بیمارانی که کنترل مناسب قند خون ندارند را نشان داده است. در حالی که بیشتر RA های GLP-1 قابل تزریقی هستند و فقط یک دارو از این گروه به نام سماگلوتید ( semaglutide) به صورت خوراکی در دسترس است. در کارآزمایی های مقایسه ای افزودن GLP-1 RA با انسولین، در بیمارانی که نیاز به کاهش بیشتر گلوکز دارند ، اثر کاهش دهندگی قند خون GLP-1 RA تزریقی مشابه یا بیشتر از انسولین پایه بوده است. GLP-1 RAs در مقایسه با انسولین اثرات مفیدی روی وزن دارد و باعث افزایش وزن نمی شود، باعث هیپوگلیسمی نمی شود ولی عوارض گوارشی بیشتری دارد. بنابراین ، مطالعات برتری آنالوگ های GLP-1 در مقایسه با انسولین در بیمارانی که نیاز به داروی تزریقی دارند را ثابت کرده اند. با این حال ، هزینه های بالا و عواض جانی و عدم تحمل از موانع مهم استفاده از GLP-1 RA هستند.
هزینه داروی دیابت طی دو دهه گذشته به طرز چشمگیری افزایش یافته است و اکنون بار زیادی را متوجه ی بیمار و خانوده اش می کند. جدول 9.2 اطلاعات مربوط به هزینه های درمان های غیرانسولین مورد تایید فعلی را ارائه می دهد. هزینه های دارویی می تواند منبع اصلی استرس برای بیماران دیابتی باشد و به استمرار در مصرف دارو را به شدت کاهش می دهد. استراتژی های کاهش هزینه ممکن است در برخی موارد پایبندی به درمان را بهبود بخشد.
نتایج مطالعات قلب و عروق
چندین مطالعه ی کنترل شده تصادفی (RCT) بزرگ وجود دارد که نشان می دهد از نظر آماری کاهش قابل توجهی در حوادث قلبی عروقی در بیماران مبتلا به دیابت نوع ۲ که تحت درمان با یک مهار کننده SGLT2 (امپاگلیفلوزین ، کاناگلیفلوزین ، داپاگلیفلوزین) یا GLP-1 RA (لیراگلوتید ، سماگلوتید ، دلاگلوتید) قرار داشته اند دیده می شود. افرادي در این مطالعات وارد شدند كه از امپگليفلوزين ، كاناگليفلوزين ، داپاگليفلوزين ، ليراگلوتييد و سماگلوتيد استفاده می کردند و A1C آنها در شروع مطالعه بیش از ۶/۵٪ بوده است و در بیش از ۷۰ درصد از متفورمین به عنوان داروی پایه استفاده می کردند. تعمیم نتایج عملی این مطالعات این است که در بیمارانی که ASCVD اثبات شده دارند و یا ریسک بالای برای ASCVD دارند یکی از این داروها باید در رژیم درمانی دیابت گنجانده شود . برای این بیماران ، استفاده از یکی از مهارکننده های SGLT2 یا GLP-1 RA با اثرات مفید اثبات شده قلبی عروقی توصیه می شود. در مطالعات قلبی عروقی ، امپاگلیفلوزین ، کاناگلیفلوزین ، داپاگلیفلوزین ، لیراگلوتید ، سماگلوتید و دولاگلوتید همه اثرات مفیدی بر شاخص های CKD داشتند .
انسولین درمانی
بسیاری از بیماران مبتلا به دیابت نوع ۲ در نهایت به انسولین درمانی نیاز پیدا می کنند و از آن بهره مند می شوند. برای راهنمایی در مورد نحوه تجویز ایمن و موثر انسولین ، به بخش تزریق انسولین در بالا مراجعه کنید. ماهیت پیشرونده دیابت نوع ۲ باید به طور منظم و عینی برای بیماران توضیح داده شود ، و ارائه دهندگان خدمات باید از استفاده انسولین به عنوان تنبیه یا توصیف آن به عنوان نشانه کوتاهی شخص در مراقبت از خود خودداری کنند. در عوض ، بر سودمندی و اهمیت انسولین برای حفظ کنترل قند خون هنگامی که پیشرفت بیماری بر داروهای خوراکی فائق آمد تاکید شود. آموزش و مشارکت بیماران در مدیریت بیماری خود و استفاده از انسولین حائز اهمیت است. به عنوان مثال ، باید به بیماران آموزش داد تا بتوانند تیتراسیون و تعیین دز متناسب با خود را یاد بگیرند. آموزش جامع در مورد نظارت بر خود بر قند خون ، رژیم غذایی ، و جلوگیری از درمان مناسب قند خون در هر بیمار با استفاده از انسولین بسیار مهم است. همچنین آموزش لازم در مورد نحوه ی آزمایش قند خون، جلو گیری از هیپوگلیسمی و درمان آن در بیمارانی که از انسولین استفاده می کنند اهمیت حیاتی دارد.
انسولین پایه
استفاده از انسولین پایه به تنهایی راحت ترین روش استفاده از انسولین است و می تواند به متفورمین و سایر عوامل خوراکی اضافه شود. دوزهای شروع را می توان بر اساس وزن بدن ( ۰/۱ تا ۰/۲ واحد به ازای هر کیلوگرم وزن بدن در روز) و درجه هیپرگلیسمی تخمین زد و با تیتراسیون طی روزها تا هفته ها به دز متناسب رسید. ماموریت انسولین پایه جلوگیری از تولید گلوکز توسط کبد و محدود کردن قند خون در طول شب و بین وعده های غذایی است. کنترل گلوکز ناشتا را می توان با انسولین NPH انسانی یا انسولین آنالوگ با اثر طولانی به دست آورد. در مطالعات بالینی ، استفاده از آنالوگهای پایه ی طولانی مدت (U-100 glargine یا detemir) در مقایسه با NPH هیپو گلیسمی علامتی و شبانه کمتری ایجاد می کنند. اگر چه این این کاهش ریسک چشمگیر نیست و ممکن است ادامه نداشته باشد. استفاده از آنالوگهای طولانی اثرتر مانند (U-300 glargine یا degludec) در مقایسه با U-100 glargine در ترکیب با داروهای خوراکی احتمال هیپوگلیسمی کمتری دارند. اگر چه کاهش احتمال هیپوگلیسمی به دنبال استفاده از این آنالوگ های طولانی اثر در مقایسه با NPH در مطالعات بالینی به اثبات رسیده است با این وجود این اختلاف ممکن است در دنیای واقعی چشمگیر نباشد. پزشکان باید از احتمال استفاده ی غیر معقول از انسولین پایه ( overbasalisation ) آگاه باشند. علائم استفاده ی زیاد و نابجا از انسولین پایه عبارتند از دز بیش ار ۰/۵ واحد به ازای هر کیلوگرم وزن بدن ، تفاوت زیاد بین قند زمان خواب با قند خون ناشتا ( به عنوان مثال تفاوت بیش از ۵۰ میلی گرم در دسی لیتر بین قند زمان خواب و قند ناشتا) و تفاوت زیاد بین قند قبل و بعد از غذا ، هیپوگلیسمی (آگاه یا ناآگاه) . در صورت وجود موارد بالا باید درمان بیمار مجددا مورد بازنگری قرار گیرد.
هزینه انسولین طی دو دهه گذشته در مقایسه با هزینه های دیگر پزشکی به به طور مداوم در حال افزایش است. این هزینه بار قابل توجهی را به بیماران تحمیل می کند زیرا انسولین برای افرادی که دیابت دارند به یک هزینه در حال رشد تبدیل شده است. این هزینه ها به طور مستقیم منجر به عدم رعایت درمان می شود. بنابراین ، در نظر گرفتن هزینه هایکی از مولفه های مهم مدیریت درمان است. برای بسیاری از بیماران مبتلا به دیابت نوع ۲ (به عنوان مثال ، افرادی با اهداف A1C متوسط، میزان پایین هیپوگلیسمی ، و مقاومت شدید به انسولین ، و همچنین کسانی که از نظر هزینه ای مشکل دارند) ، انسولین انسانی (NPH و رگولار ) ممکن است انتخاب مناسب درمان باشد ، و پزشکان باید با کاربرد آنها آشنا باشند. انسولین رگولار انسانی ، NPH و 70/30 NPH را می توان با قیمت کمتری از داروخانه ها تهیه کرد.
انسولین قبل غذا
بسیاری از افراد مبتلا به دیابت نوع ۲ برای رسیدن به اهداف مناسب قند خون ، علاوه بر انسولین پایه ، به دوز انسولین قبل از غذا نیز نیاز دارند. دوز ۴ واحد یا ۱۰٪ مقدار انسولین پایه در بزرگترین وعده غذایی یا وعده غذایی با بیشترین افزایش قند خون شروع می شود. سپس رژیم انسولین را می توان بر اساس نیاز بیمار تشدید کرد. افراد مبتلا به دیابت نوع ۲ به طور کلی مقاومت بیشتری به انسولین نسبت به افراد مبتلا به دیابت نوع ۱ دارند ، بنابر این به دوزهای روزانه بالاتری ((1 واحد / کیلوگرم) نیاز دارند و به میزان کمتری مبتلا به هیپوگلیسمی می شوند. تیتراسیون می تواند براساس اندازه گیری قند خانگی یا A1C باشد. با افزودنهای قابل توجه به دوز انسولین جمعی ، به ویژه در وعده عصرانه ، باید به کاهش انسولین پایه توجه شود. متاآنالیز مطالعات مقایسه ای استفاده از انسولین سریع اثر آنالوگ با انسولین رگولار انسانی در بیماران دیابتی نوع ۲ تفاوت قابل توجهی در میزان A1C یا میزان بروز هیپوگلیسمی نشان نمی دهند.
انسولین غلیظ
در حال حاضر چندین داروی غلیظ انسولین موجود است. انسولین رگولار U-500 ، طبق تعریف ، پنج برابر غلیظ تر از انسولین رگولار U-100 است. U-500 رگولار دارای فارماکوکینتیک مشخص با شروع تأخیری و مدت زمان طولانی تر نسبت به رگولار U-100 است ، دارای خصوصیاتی بیشتر شبیه انسولین اثر متوسط (NPH) است و می تواند در دو یا سه تزریق روزانه استفاده شود. غلظت U-300 گلارژین و U-200 degludec سه و دو برابر بیشتر از فرمولاسیون های U-100 آنها است و اجازه می دهد دوزهای بالاتر تجویز انسولین پایه در هر حجم واحداستفاده شود. گلارژین U-300 دارای مدت زمان طولانی تری نسبت به U-100 گلارژین است اما نسبت به واحد تجویز اثر متوسط نسبتاً کمتری دارد. FDA همچنین فرمولاسیون غلیظ انسولین سریع اثر لیزپرو ، U-200 (200 واحد در میلی لیتر) و انسولین lispro-aabc (U-200) را تأیید کرده است. تزریقاین داروهای غلیظ ممکن است برای بیماران راحت ترباشد و ممکن است در کسانی که مقاومت به انسولین دارند و به دوزهای زیادی انسولین نیاز دارند ، میزان پایبندی را بهبود ببخشند. در حالی که انسولین معمولی U-500 در هر دو قلم و ویال موجود است ، سایر انسولین های غلیظ فقط در قلم های پر شده در دسترس هستند تا خطر خطاهای دوز را به حداقل برسانند.
انسولین استنشاقی
انسولین استنشاقی به عنوان انسولین سریع اثر در دسترس است. مطالعات انجام شده در افراد مبتلا به دیابت نوع ۱ فارماکوکینتیک سریع را نشان می دهد . دریک مطالعه موردی شواهدی نشان داده شده که در مقایسه با انسولین تزریقی سریع اثر ، دوزهای اضافی انسولین استنشاقی بر اساس میزان قند خون بعد از غذا می تواند باعث بهبود قند خون بدون افزایش خطر هیپوگلیسمی یا افزایش وزن شود ، اگرچه برای تأیید نتایج یک مطالعه بزرگتر لازم است . انسولین استنشاقی در بیماران مبتلا به بیماری مزمن ریوی مانند آسم و بیماری انسدادی مزمن ریوی منع مصرف دارد و در بیمارانی که سیگار می کشند یا اخیراً سیگار را ترک کرده اند توصیه نمی شود. همه بیماران برای شناسایی بیماری بالقوه ریه قبل و بعد از شروع انسولین درمانی استنشاق به اسپیرومتری نیاز دارند.
درمان تزریقی ترکیبی
اگر انسولین پایه به میزان قابل قبول قند خون ناشتا را کاهش داده باشد و یا اگر دوز مصرفی به بیش از ۰/۵ واحد در کیلوگرم در روز رسیده باشد ولی A1C بالاتر از حد هدف باقی مانده باشد، درمان تزریقی ترکیبی را درنظر بگیرید. در این روش می تواند از یک GLP-1 RA اضافه شده به انسولین پایه یا دوزهای مختلف انسولین استفاده کرد.. ترکیبی از انسولین پایه و GLP-1 RA دارای قدرت کاهش دهندگی قوی قند به همراه افزایش وزن کمتر در مقایسه با رژیم های تشدیده شده ی انسولین است. در یک مطالعه دوام بیشتر ثبات قند خون در مقایسه با افزودن انسولین پایه به تنهایی دیده شده است. دو محصول مختلف با ترکیب دوتایی ثابت و مصرف یک بار در روز حاوی انسولین پایه به همراه GLP-1 RA موجود است: انسولین گلارژین به علاوه لیکسیسناتید با نام تجاری سولیکووا(Soliqua) و انسولین دگلودک به اضافه لیراگلوتید با نام تجاری ترسیبا ( Tresiba).
تشدید درمان انسولین را می توان با افزودن دوزهای پراندیال به انسولین پایه انجام داد. شروع با یک تزریق قبل از بزرگترین وعده ی غذای انجام می شود و در صورت لزوم می توان آن را به یک رژیم با پند تزریق قبل از وعده های غذایی افزایش داد ( MDI). در روش دیگر ، در یک بیمار که به دز واحد انسولین پایه جواب مناسب نمی دهد و A1C به هدف نمی رسد می توان از ترکیب انسولین های مخلوط آماده با تزریق دوبار در روز استفاده کرد. هر رویکرد مزایا و معایبی دارد. به عنوان مثال ، رژیم های پایه و بولوس انعطاف پذیری بیشتری برای بیمارانی که برنامه های غذای نامنظمی دارند ارائه می دهند. از طرف دیگر ، دو دوز انسولین مخلوط شده یک وسیله ساده و راحت برای تزریق انسولین در طول روز است. علاوه بر این ، انسولین های انسانی ، به طور جداگانه ، مخلوط شده توسط خود بیمار ، یا به عنوان فرمول های پیش ساخته NPH / رگولار ( ۷۰/۳۰) ، گزینه های کم هزینه تری در مقایسه با ترکیبات آنالوگ هستند. هنگام شروع درمان تزریقی ترکیبی ، درمان با متفورمین باید حفظ شود ، در حالی که سولفونیل اوره و مهار کننده های DPP-4 معمولاً قطع می شوند. در بیماران با کنترل کمتر از حد مطلوب قند خون ، به ویژه در مواردی که به دوزهای انسولین زیادی نیاز دارند ، استفاده اضافی از تیازولیدین دیون یا یک مهار کننده SGLT2 ممکن است به بهبود کنترل و کاهش میزان انسولین مورد نیاز کمک کند ، اگرچه عوارض جانبی بالقوه باید در نظر گرفته شود.
تصویر دوم
درمان دارویی برای دیابت نوع 1
توصیه ها
اکثر افراد مبتلا به دیابت نوع ۱ باید با تزریق روزانه چندین نوبت از انواع انسولین شامل یک دز انسولین پایه و ۳ نوبت انسولین قبل وعده های غذایی (MDI) و یا تزریق مداوم انسولین زیر جلدی توسط پمپ ( pump therapy) تحت درمان قرار گیرند.
اکثر افراد مبتلا به دیابت نوع ۱ برای کاهش خطر افت قند خون ( هیپوگلیسمی ) باید از انسولین سریع اثر آنالوگ استفاده کنند.
بیماران مبتلا به دیابت نوع ۱ باید در مورد چگونگی مطابقت دوزهای انسولین قبل غذا با مقدار کربوهیدرات موجود در غذا ، گلوکز قبل از غذا و میزامفعالیت بدنی آموزش ببینند.
انسولین درمانی ( insulin therapy )
از آنجا که مشخصه اصلی دیابت نوع ۱ اختلال شدید در عملکرد سلول β و یا از بین رفتن کامل فعالیت آن است بنابر این در بدن مبتلایان تقریباً انسولین به طور طبیعی وجود ندارد و تجویز انسولین ضروری است. علاوه بر افزایش قند خون ، عدم وجود انسولین می تواند منجر به سایر اختلالات متابولیکی مانند افزایش چربی های خون ( هیپرتری گلایسیریدمی) و کتواسیدوز و همچنین کاتابولیسم بافت های بدن و تهدید زندگی باشد. در طی شش یا هفت دهه پس از کشف انسولین ، با استفاده از تزریق یک و یا دوبار انسولین از بوجود آمدن این عوارض جلوگیری می شد. . با این وجود ، طی سه دهه گذشته ، با جمع آوری شواهد نشان داده شد که جایگزینی شدید انسولین با استفاده از چندین تزریق روزانه و یا تجویز زیر جلدی مداوم از طریق پمپ انسولین ، بهترین و مطمئن ترین راه برای درمان مبتلایان به دیابت نوع ۱ است. نتایج مطالعه ی DCCT نشان داد که درمان شدید با تزریق چند دز روزانه و یا تزریق مداوم زیر جلدی انسولین (CSII) A1C را کاهش می دهد و با بهبود نتایج طولانی مدت همراه است. این مطالعه با انسولین های انسانی کوتاه اثر (رگولار) و متوسط اثر (NPH) انجام شد. بر اساس نتایج این مطالعه ی مهم ، A1C پایین تر با کنترل شدید (7٪) (intensive control) منجر به کاهش 50٪ در عوارض میکرو واسکولار در طی 6 سال درمان شد. با این حال ، درمان شدید با میزان بالاتر کاهش شدید قند خون ( هیپوگلیسمی ) نسبت به درمان معمولی همراه بود (62 در مقایسه با 19 مورد در هر 100 بیمار در یک سال درمان). پیگیری افراد مورد مطالعه ی DCCT برای بیش ۱۰ سال پس از پایان پروژه نشان داد افرادی که تحت درمان شدید قرار داشته اند به مراتب کمتر دچار عوارض ماکرو واسکولار و میکروواسکولار شده اند.
در طول ۲۵ سال گذشته ، انسولین های آنالوگ کوتاه اثر و طولانی اثر پا به عرصه ی ظهور نهاده اند که دارای اثرات فارماکوکینتیک و فارماکو دینامیک متفاوت با انسولین های انسانی قبلی هستند. انسولین های آنالوگ پایه (basal ) دارای مدت زمان طولانی تری با غلظت پلاسما یی ثابت تر نسبت به انسولین NPH هستند. آنالوگهای سریع اثر (RAA) نسبت به انسولین انسانی معمولی ( regular) داری شروع اثر و اوج سریع تر و مدت زمان کوتاهتر هستند. در افراد مبتلا به دیابت نوع 1 ، استفاده از انسولین های آنالوگ باعث کاهش شدید کمتر قند خون ( هیپوگلیسمی ) ، افزایش وزن کمتر و همچنین A1C پایین تر در مقایسه با انسولین های انسان می شود. اخیراً ، دو فرمول جدید انسولین با پروفیل های عمل سریع تر معرفی شده است. انسولین انسانی استنشاقی در مقایسه با RAA دارای اوج سریع تر و مدت زمان اثر کوتاه تری است و ممکن است باعث کاهش کمتر در بروز هیپوگلیسمی و افزایش وزن کمتری شود .انسولین آسپارت انسولین با اثر سریعتر faster acting insulin aspart و انسولین لیسپرو سریع اثر ( lipro-aabc ) ممکن است در کنترل افزایش قند بعد غذا بهتر از RAA عمل کنند. برای روشن میزان اثر این نوع انسولین ها در درمان و مدیریت دیابت به تحقیقات بیشتری نیاز است. علاوه بر این ، آنالوگهای جدید با عملکرد طولانی تر (U-300 گلارژین یا دگلودک degludec) ممکن است در مقایسه با U-100 گلارژین در بیماران مبتلا به دیابت نوع ۱ هیپوگلیسمی کمتری ایجاد کنند. با وجود مزایای انسولین های آنالوگ در درمان مبتلایان به دیابت نوع ۱ ، ممکن است قیمت و هزینه های این انسولین ها موانعی برای مصرف آنها در بعضی از بیماران ایجاد کند. رویکردهای متعددی برای درمان با انسولین وجود دارد ولی هدف تمام آنها کنترل قند خون با حداقل بروز هیپوگلیسمی، جلوگیری از بروز کت و اسیدوز، جلوگیری از بوجود آمدن عوارض و کنترل قند خون در حد امکان در محدوده ی طبیعی است.
بیشتر مطالعات برای مقایسه ی چندین تزریق روزانه (MDI) با درمان با پمپ (CSII ) نسبتاً کوچک و با مدت زمان کوتاه بوده اند. با این حال ، یک بررسی سیستماتیک و متاآنالیز اخیر به این نتیجه رسیده است که پمپ درمانی دارای مزایای متوسطی در مقایسه با MDI برای کاهش A1C (.0.30) و کاهش میزان شدید افت قند خون در کودکان و بزرگسالان است . با این حال ، هیچ اتفاق نظری برای انتخاب تزریق یا پمپ درمانی در یک بیمار معین وجود ندارد و تحقیقات بیشتری برای رسیدن به تصمیم گیری صحیح لازم است. تاثیرات مثبت مانیتورهای مداوم گلوکز در مدیریت قند خون Glucose monitoring system در بسیاری از موارد به اثبات رسیده است. استفاده از سنسورهای گلوکز با قطع خودکار انسولین در بیمارانی که از CSII استفاده می کنند می تواند منجر به کاهش هیپوگلیسمی شبانه شود. هنگام انتخاب از بین روش های مختلف انسولین درمانی باید مواردی مانند ترجیح بیمار ، هزینه و نوع انسولین مصرفی نظر گرفته شود.
سازمان غذا و داروی ایالات متحده (FDA) اکنون دو سیستم پمپ حلقه بسته ترکیبی ( hybrid closed-loop pump systems)را تأیید کرده است. ایمنی و کارآیی این سیستم ها در نوجوانان و بزرگسالان مبتلا به دیابت نوع 1 نشان داده شده است. و شواهد اخیر نشان می دهد که hybrid closed-loop pump systems در مقایسه با ترکیب پمپ همراه با سنسور در کنترل قند خون و کاهش هیپوگلیسمی در یک دوره ی ۳ ماهه در کودکان و بزرگسالان مبتلا به دیابت نوع 1 مفید تر بوده است. در مطالعه ی International Diabetes Closed Loop (iDCL) ، در یک دوره ی 6 ماهه در بیماران دیابتی نوع 1 با سن حداقل ۱۴ سال، استفاده از closed loop در مقایسه با پمپ درصد بیشتری از بیماران در میزان قند خون تعیین شده ی هدف بوده اند ، متوسط قند خون و A1C پایین تری داشته اند و مدت زمان کمتری در هیپوگلیسمی بوده اند.
درمان شدید دیابت با استفاده از پمپ و پایش مداوم قند خون در بیشتر بیماران نوع ۱ دیابت باید در نظر گرفته شود. سیستمهای تزریق خودکار انسولین ممکن است در بزرگسالان مبتلا به دیابت نوع 1 که مهارت لازم برای استفاده از آنها را دارند به منظور دستیابی به بیشترین زمان نگه داشتن قند خون در محدوده ی طبیعی، کاهش A1C و هیپوگلیسمی کمتر مد نظر قرار گیرند.
به طور کلی ، بیماران مبتلا به دیابت نوع 1 به ۵۰٪ انسولین روزانه به عنوان پایه و ۵۰٪ به صورت قبل از وعده های غذایی نیاز دارند. کل نیاز روزانه به انسولین را می توان بر اساس وزن تخمین زد. نیاز روزانه ی این بیماران حدود ۴/ تا ۱ واحد به ازای هر کیلو گرم وزن است. به مقادیر بیشتری در دوران بلوغ ، بارداری و بیماری ها نیاز است. انجمن دیابت آمریکا دز ۰/۵ واحد به ازای هر کیلو گرم وزن بدن را در بیمارانی که از نظر متابولیک در شرایط پایدار هستند پیش نهاد می کند. نیمی از آن به عنوان انسولین پایه برای کنترل قند خون در بین وعده های غذایی و نیم دیگر به عنوان انسولین قبل غذا برای کنترل قند بعد از غذا تجویز می شود.
در رژیم های چند وعده ای معمولی برای بیماران مبتلا به دیابت نوع 1 ، انسولین های کوتاه اثر را قبل از وعده های غذای و انسولین پایه را غالبا در شب تزریق می کنند. زمان مناسب برای تجویز انسولین قبل غذا ، بر اساس فارماکوکینتیک فرمولاسیون ( رگولار ، RAA ، استنشاقی) ، سطح گلوکز قبل از غذا و مصرف کربوهیدرات متفاوت است. ترشح انسولین فیزیولوژیک با میزان قند خون ، اندازه وعده غذایی و نیازهای بافتی به گلوکز متفاوت است. بنابراین ، آموزش به بیماران در مورد چگونگی تنظیم انسولین قبل غذا با در نظر گرفتن مصرف کربوهیدرات ، سطح گلوکز قبل از غذا و فعالیت پیش بینی شده می تواند موثر باشد و باید به اکثر بیماران ارائه شود. برای افرادی که از شمارش کربوهیدرات استفاده می کنند ، تخمین میزان چربی و پروتئین وعده های غذایی را می توان در دوز اصلی آنها برای سود بیشتر وارد کرد.
روش تزریق انسولین
اطمینان از درک صحیح روش تزریق انسولین توسط بیماران و یا مراقبان ، برای بهبود کنترل قند خون بسیار مهم است. بنابراین مهم است که انسولین به روش صحیح به داخل بافت مناسب تزریق شود. منابع زیادی برای فرا گیری روش تزریق انسولین در دسترس است. نکات مهم در تزریق مناسب انسولین عبارتند از تزریق به مناطق مناسب بدن ، چرخش محل تزریق ، مراقبت های مناسب از محل های تزریق برای جلوگیری از عفونت یا عوارض دیگر و جلوگیری از تزریق انسولین به روش عضلانی است.
انسولین باید در بافت زیرپوستی تزریق شود و در داخل عضله تزریق نشود. محل های توصیه شده برای تزریق انسولین عبارتند از شکم ، ران ، باسن و بالای بازو . از آنجا که جذب انسولین در تزریق عضلانی با توجه به فعالیت عضله متفاوت است ممکن است منجر به نتایج غیرقابل پیش بینی و هیپوگلیسمی مکرر در سطح قند خون شود. خطر تزریق انسولین عضلانی در کودکان و افراد لاغر در هنگام تزریق به اندام ها به جای تنه (شکم و باسن) و استفاده از سوزن های بلند به مراتب بالاتر است. شواهد اخیر نشان داده است که استفاده از سوزن های کوتاه (به عنوان مثال ، سوزن های قلم 4 میلی متری) در مقایسه با سوزن های بلند تر ، به عنوان روشی موثر و قابل اعتماد در تزریق انسولین حتی در افراد چاق مفید هستند.
چرخش محل تزریق می تواند از لیپوهیپرتروفی بافت چربی که به علت اثر چربی زایی ( لیپوژنسیتی ) انسولین به علت تزریق مکرر در یک محل است ، جلوگیری کند. لیپوهیپرتروفی به صورت نواحی منظم و نرم چند سانتی متری ظاهر می شود و می تواند باعث جذب نامنظم انسولین و در نتیجه نتایج غیر قابل پیش بینی در سطح قند خون شود. بیماران و یا مراقبان آنها باید در مورد اهمیت تزریق چرخشی در تنظیم و کنترل قند خون آموزش های لازم را ببینند. بیماران باید در هر مراجعه از نظر محل تزریق انسولین و وجود و یا عدم وجود هیپرتروفی مورد معاینه قرار بگیرند ، وسیله ی تزریق آنها مانند سرنگ و یا قلم مورد بازدید واقع شود و در مورد استفاده ی صحیح آن ارزیابی شوند .
درمان های غیر انسولین برای دیابت نوع 1
اثر بخشی داروهای تزریقی و خوراکی مختلف به عنوان مکمل های درمان انسولین برای دیابت نوع 1 مورد مطالعه قرار گرفته اند
پراملینتید ( pramlintide) : بک آنالوگ هورمون آمیلین ( amylin) است که به طور طبیعی از سلولهای بتا پانکراس ترشح می شود. ابن دارد برای استفاده در بزرگسالان مبتلا به دیابت نوع 1 مورد تایید FDA قرار گرفته است. نتایج حاصل از مطالعات کنترل شده تصادفی ( RCT) ، نشان داده است که افزودن این دارو به انسولین باعث کاهش A1C (بین ۰ تا ۳/ درصد) و کاهش وزن بدن (1–2 کیلوگرم) می شود.
متفورمین: افزودن متفورمین در بزرگسالان مبتلا به دیابت نوع ۱ باعث کاهش اندکی در وزن بدن و سطح چربی های خون می شود اما تاثیری در بهبود A1C ندارد.
آنالوگ های GLP-1 :افزودن این داروها مانند لیراگلوتید ( Liraglutide )یا اگزناتید ( Exenetide) به انسولین درمانی باعث کاهش اندکی در A1C ( به میزان ۲/ درصد ) در مقایسه با انسولین به تنهایی در افراد مبتلا به دیابت نوع ۱ و همچنین کاهش وزن بدن ( حدود ۳ کیلوگرم ) می شوند.
مهار کننده های SGLT-2
افزودن این داروها به انسولین باعث بهبود A1C و کاهش وزن بدن در مقایسه با انسولین به تنهایی می شوند . با این حال ، استفاده از مهار کننده های SGLT2 در دیابت نوع ۱ با افزایش دو تا چهار برابر کتواسیدوز همراه است. به خاطر داشته باشید فقط پراملینتاید برای درمان دیابت نوع ۱ تأیید می شود.
درمان جراحی برای دیابت نوع ۱
پیوند لوزالمعده و جزایر
پیوند موفقیت آمیز پانکراس و یا جزایر بتا می تواند باعث عادی شدن قند خون شود و عوارض عروقی دیابت نوع ۱ را کاهش دهد. با این حال ، بیمارانی که از این روش های درمانی استفاده می کنند برای جلوگیری از رد پیوند و یا عود تخریب جزایر بتا ی خود ملزم به استفاده از داروهای سرکوبگر سیستم ایمنی به صورت مادام العمر هستند. با توجه به عوارض جانبی بالقوه درمان سرکوب سیستم ایمنی ، پیوند پانکراس فقط باید برای بیماران مبتلا به دیابت نوع ۱ که به طور همزمان نیاز به پیوند کلیه دارند و یا قبلا مورد پیوند کلیه قرار گرفته اند مد نظر قرار گیرد. همچنین در بیمارانی که کتواسیدوز مکرر دارند و یا افت مکرر و شدید قند خون دارند نیز کمک کننده است.
درمان دارویی برای دیابت نوع ۲
توصیه ها
۱- متفورمین داروی اولیه و ترجیحی برای درمان دیابت نوع ۲ است.
۲- متفورمین پس از شروع ، باید تا زمانی که تحمل شود و منع مصرف نداشته باشد ، ادامه یابد. سایر عوامل ، از جمله انسولین ، باید به متفورمین اضافه شوند.
۳- درمان ترکیبی چند دارویی اولیه می تواند در برخی از بیماران هنگام شروع درمان در نظر گرفته شود تا شکست درمان کاهش یابد.
۴- در صورت شواهدی مبنی بر کاتابولیسم مداوم (کاهش وزن) و یا علائم هیپرگلیسمی شدید و یا مقدار A1C بیش از ۱۰ درصد و یا مقدار قند خون بیش یا مساوی ۳۰۰ میلی گرم در دسی لیتر ، شروع انسولین به عنوان اولین خط درمان باید مورد توجه قرار گیرد.
۵- در انتخاب عوامل دارویی باید از رویكرد بیمار محور استفاده شود. ملاحظاتی مانند تأثیر دارو روی بیماریهای قلبی عروقی و کلیوی ، میزان اثربخشی ، خطر افت قند خون ، تأثیر بر وزن ، هزینه ، خطر ابتلا به عوارض جانبی و ترجیح بیمار در انتخاب نوع دارو باید مد نظر قرار گیرند.
۶- بیماران مبتلا به دیابت نوع ۲ که بیماری قلبی عروقی آترواسکلروتیک (ASCVD) دارند یا شاخص های خطر بالا دارند و یا بیماری کلیوی یا نارسایی قلبی دارند ، یک مهار کننده گیرنده ی پمپ سدیم-گلوکز کوتراسپانسر ۲ (SGLT2 inhibitors ) و یا آگونیست های گیرنده پپتید ۱ (GLP-1 analogue ) با مزایای بیماری قلبی عروقی ثابت شده، به عنوان بخشی از رژیم دارویی کنترل قند خون مستقل از A1C و با در نظر گرفتن فاکتورهای خاص باید مد نظر قرار گیرند.
۷- در بیماران دیابتی نوع ۲ ، آگونیست گیرنده پپتید ۱ ( GLP-1 analogue) ، در صورت امکان به انسولین ترجیح داده می شود.
۸- تشدید درمان برای بیمارانی که به اهداف درمانی توصیه شده نمی رسند نباید به تأخیر بیفتد.
۹- رژیم دارویی و نحوه ی مصرف دارو باید در فواصل منظم (هر ۳ تا ۶ ماه یک بار) ارزیابی مجدد شود و در صورت لزوم تغییرات لازم انجام شود.
۱۰- پزشکان باید از خطرات استفاده ی بیش از حد از انسولین پایه (overbasalization) آگاهی داشته باشند. نشانه های استفاده ی بیش از مقدار انسولین پایه عبارتند از مصرف بیش از ۵/ ( نیم واحد) انسولین پایه به ازای هر کیلوگرم وزن بدن، تفاوت زیاد بین مقدار قند خون قبل خواب و صبح ناشتا، تفاوت زیاد بین قند خون قبل و بعد از غذا و افت های مکرر قند خون ( با آگاهی و یا بدون آگاهی ) در شبانه روز. در صورت وجود موارد بالا نوع درمان بیمار باید مورد ارزیابی مجدد قرار بگیرد.
درمان اولیه
متفورمین باید در زمان تشخیص دیابت نوع ۲ به عنوان اولین دارو شروع شود مگر اینکه موارد منع مصرف وجود داشته باشد. برای بسیاری از بیماران ، این درمان مونوتراپی در ترکیب با اصلاح سبک زندگی موثر خواهد بود. داروهای اضافی و یا جایگزین ممکن است در شرایط خاص در نظر گرفته شوند ، مانند افرادی که بیماریهای قلبی عروقی و یا کلیوی دارند. متفورمین موثر و بی خطر و ارزان است و ممکن است خطر حوادث قلبی عروقی و مرگ را کاهش دهد. متفورمین به دو صورت جذب فوری برای دوز دو بار در روز و فرم آهسته رهش که می تواند یک بار در روز تجویز شود در دسترس است. در مقایسه با سولفونیل اوره ، متفورمین به عنوان درمان خط اول اثرات مفیدی بر A1C ، وزن و مرگ و میر قلبی عروقی دارد. شواهد سیستماتیک کمی برای سایر داروهای خوراکی به عنوان درمان اولیه دیابت نوع ۲ در دسترس است.
عوارض اصلی متفورمین عبارتند از نفخ ، ناراحتی شکمی و اسهال. این موارد را می توان با کاهش دوز و افزایش تدریجی آن از بین برد. این دارو با فیلتراسیون از کلیه دفع می شود بنابر این در مواردی مانند کاهش حجم و یا فشار خون و یا نارسایی کلیه ها می تواند در بدن انباشت شود و منجر به لاکتیک اسیدوز شود. با این حال ، احتمال وقوع این عارضه بسیار نادر است . FDA برچسب متفورمین را اصلاح کرده است و استفاده از آن را در بیمارانی که eGFR بیش و یا مساوی ۳۰ میلی لیتر در دقیقه به ازای ۱/۷۳ متر مربع سطح بدن دارند مجاز شمرده است. یکمطالعه ی RCT مشاهدات قبلی در مورد وقوع کمبود ویتامین B12 در بیمارانی که از متفورمین استفاده می کنند را تایید کرده است. استفاده از متفورمین با کمبود ویتامین B12 و بدتر شدن علائم نوروپاتی مرتبط است. این یافته ها با گزارشی از مطالعه نتایج پیشگیری از دیابت (DPPOS) سازگار است که آزمایش دوره ای ویتامین B12 را پیشنهاد می کند.
در بیماران با موارد منع مصرف یا عدم تحمل متفورمین ، درمان اولیه باید بر اساس عوامل بیمار محور باشد. دارویی را از کلاس دیگری که در شکل 9.1 نشان داده شده در نظر بگیرید. وقتی A1C بیش یا مساوی ۱/۵٪ از اهداف درمانی بالاتر باشد در اغلب بیماران به دو دارو به عنوان شروع درمان برای رسیدن به اهداف درمانی نیاز است. انسولین این مزیت را دارد که در مواردی که داروهای دیگر در کنترل قند خون موثر نیستند موثر است . در موارد افزایش شدید قند خون انسولین باید جزئی از هر نوع ترکیب دارویی باشد. خصوصاً اگر ویژگی های کاتابولیک (کاهش وزن ، هیپرتری گلیسیریدمی ، کتوز) وجود داشته باشد. در بیمارانی که با قند خون برابر و یا بیش از ۳۰۰ میلی گرم در دسی لیتر دارند و یا A1C بیش از ۱۰٪ است و یا علایم افزایش شدید قند خون مانند پر نوشی و پر ادراری وجود دارد و یا شواهدی برای کاتابولیسم و شکیت بافت های بدن مانند کاهش وزن وجود دارد به عنوان خط اوا درمان باید مورد استفاده قرار بگیرد. در اغلب موارد با برطرف شدن مسمومیت گلوکز تغییر به روشهای ساده تر درمان مانند تغییر به داروهای خوراکی امکان پذیر است. با این حال ، شواهدی وجود دارد که بیماران مبتلا به هایپرگلیسمی کنترل نشده همراه با دیابت نوع ۲ را می توان به طور موثر با سولفونیل اوره نیز درمان کرد.
ترکیبی درمانی
از آنجا که دیابت نوع ۲ در بسیاری از بیماران یک بیماری پیشرونده است ، حفظ اهداف قند خون با مونوتراپی در اغلب موارد فقط برای چند سال امکان پذیر است و پس از آن درمان ترکیبی لازم می شود. بر اساس توصیه های فعلی داروها را باید به صورت مرحله ای به متفورمین برای حفظ A1C در محدوده ی هدف افزود. . این روش امکان ارزیابی واضحتر از تأثیرات مثبت و منفی داروهای جدید را فراهم می کند و خطر و هزینه بیمار را کاهش می دهد. بر اساس این عوامل ، افزودن متوالی عوامل خوراکی به متفورمین استاندارد مراقبت بوده است. با این حال شواهدی وجود دارد که نشان می دهد استفاده از داروهای ترکیبی از همان ابتدا ممکن است رسیدن به اهداف درمانی را سریعتر و مدت زمان کنترل قند خون را طولانی تر کند. بر اساس مطالعه ی VERIFY (اثر Vildagliptin در ترکیب با metformin برای درمان اولیه دیابت نوع ۲) نشان داده است که درمان ترکیبی اولیه نسبت به افزودن متوالی داروها در رسیدن سریع تر به اهداف درمانی و افزایش طول مدت کنترل قند خون ارجحیت داشته است. بر اساس مطالعه ی VERIFY ، شرکت کنندگانی که ترکیب اولیه متفورمین و مهارکننده دیپپتیدیل پپتیداز ۴ (DPP-4) ویلداگلیپتین را دریافت می کردند ، کاهش کنترل قند خون در مقایسه با متفورمین به تنهایی و ویلداگلیپتین که به ترتیب به متفورمین اضافه می شود ، کاهش کندتری در مدت کنترل قند خون دارند. این نتایج را نمی توان به غیر از ویلداگلیپتین به داروهای خوراکی دیگر تعمیم داده ، اما نشان می دهند که درمان زودرس شدیدتر فوایدی دارد و باید در صورت لزوم از طریق یک فرآیند تصمیم گیری مشترک با بیماران در نظر گرفته شود. علاوه بر این ، از آنجا که اثربخشی مطلق اکثر داروهای خوراکی به ندرت از ۱٪ فراتر می رود ، درمان ترکیبی اولیه باید در بیمارانی که دارای سطح A1C برابر یا بیش از ۱/۵ تا ۲٪ بالاتر از هدف هستند ، در نظر گرفته شود.
روش های تشدید درمان برای بیمارانی که اهداف درمانی را برآورده نمی کنند نباید به تأخیر بیفتد. تصمیم گیری مشترک در بحث های مربوط به تشدید درمان مهم است. انتخاب دارویی که به متفورمین اضافه می شود براساس مشخصات بالینی بیمار و ترجیحات وی است. از ویژگی های مهم بالینی می توان به وجود ASCVD یا شاخص های مشخص شده در مورد خطر بالای ASCVD ، نارسایی قلبی ، CKD ، سایر بیماری های همراه و خطر برای اثرات جانبی دارویی خاص و همچنین ایمنی ، تحمل و هزینه اشاره کرد. اگرچه مطالعات متعددی وجود دارد که درمان دوگانه را فقط با متفورمین مقایسه می کند ، اما شواهد کمی وجود دارد که بتواند ترکیبی را با ترکیب دیگر مقایسه کند. یک متاآنالیز اثربخشی مقایسه ای نشان می دهد که هر گروه جدید از داروهای غیر انسولینی که به درمان اولیه با متفورمین اضافه می شوند ، A1C را تقریباً ۰/۷ تا ۱٪ کاهش می دهد. اگر هدف A1C تقریباً بعد از ۳ ماه محقق نشود ، متفورمین را می توان با هر یک از شش گزینه درمانی ترکیب کرد: سولفونیل اوره ، تیازولیدیندیون ، مهار کننده DPP-4 ، آنالوگ های جی ال پی 1 - GLP ، مهار کننده SGLT2 یا انسولین پایه. برای انتخاب نوع دارو باید مشخصات دارو و بیمار را در نظر گرفت.
برای بیماران مبتلا به ASCVD یا شاخص های خطرناک بالا برای ASCVD (مانند بیماران با سن بیش یا برابر ۵۵ سال مبتلا به تنگی عروق کرونر ، کاروتید یا شریان اندام تحتانی به میزان بیش از ۵۰ ٪ یا هیپرتروفی بطن چپ) ، نارسایی قلبی یا CKD ، آنالوگ های جی ال پی 1 - GLP و مهار کننده SGLT2 با اثرات مفید ثابت شده مستقل از استفاده از متفورمین و یا میزان A1C توصیه می شود. برای بیمارانی که ASCVD آنها مشخص نیست ، شاخص های خطر بالای ASCVD ، نارسایی قلبی یا CKD ندارند انتخاب عامل دوم برای افزودن به متفورمین هنوز توسط شواهد تجربی مقایسه نشده است و انتخاب دارو براساس اثربخشی ، جلوگیری از عوارض جانبی (به ویژه کاهش قند خون و افزایش وزن) ، هزینه و ترجیحات بیمار است. ملاحظات مشابه در بیمارانی که برای رسیدن به اهداف قند خون به عامل سوم نیاز دارند ، اعمال می شود. یک بررسی سیستماتیک و متاآنالیز نشان می دهد بیشترین کاهش در سطح A1C مربوط به رژیم های است که انسولین و یا انالوگ های GLP-1 به متفورمین اضافه می شوند. در همه موارد ، رژیم های درمانی باید به طور مداوم از نظر اثر بخشی ، عوارض جانبی و هزینه برای بیمار بررسی شوند. در برخی موارد ، بیماران نیاز به کاهش یا قطع دارو دارند. دلایل رایج این امر عبارتند از: عدم تأثیر ، عوارض جانبی غیر قابل تحمل ، هزینه یا تغییر در اهداف درمانی.
نیاز به افزودن داروهای تزریقی ، به ویژه در افرادی که مدت بیشتری دیابت دارند ، معمول است. افزودن انسولین پایه ، NPH انسانی و یا یکی از آنالوگهای انسولین با اثر طولانی مدت ، به رژیمهای خوراکی یک رویکرد کاملاً ثابت در درمان دیابت است که برای بسیاری از بیماران موثر است. علاوه بر این ، شواهد اخیر قابلیت استفاده از GLP-1 RA در بیمارانی که کنترل مناسب قند خون ندارند را نشان داده است. در حالی که بیشتر RA های GLP-1 قابل تزریقی هستند و فقط یک دارو از این گروه به نام سماگلوتید ( semaglutide) به صورت خوراکی در دسترس است. در کارآزمایی های مقایسه ای افزودن GLP-1 RA با انسولین، در بیمارانی که نیاز به کاهش بیشتر گلوکز دارند ، اثر کاهش دهندگی قند خون GLP-1 RA تزریقی مشابه یا بیشتر از انسولین پایه بوده است. GLP-1 RAs در مقایسه با انسولین اثرات مفیدی روی وزن دارد و باعث افزایش وزن نمی شود، باعث هیپوگلیسمی نمی شود ولی عوارض گوارشی بیشتری دارد. بنابراین ، مطالعات برتری آنالوگ های GLP-1 در مقایسه با انسولین در بیمارانی که نیاز به داروی تزریقی دارند را ثابت کرده اند. با این حال ، هزینه های بالا و عواض جانی و عدم تحمل از موانع مهم استفاده از GLP-1 RA هستند.
هزینه داروی دیابت طی دو دهه گذشته به طرز چشمگیری افزایش یافته است و اکنون بار زیادی را متوجه ی بیمار و خانوده اش می کند. جدول 9.2 اطلاعات مربوط به هزینه های درمان های غیرانسولین مورد تایید فعلی را ارائه می دهد. هزینه های دارویی می تواند منبع اصلی استرس برای بیماران دیابتی باشد و به استمرار در مصرف دارو را به شدت کاهش می دهد. استراتژی های کاهش هزینه ممکن است در برخی موارد پایبندی به درمان را بهبود بخشد.
نتایج مطالعات قلب و عروق
چندین مطالعه ی کنترل شده تصادفی (RCT) بزرگ وجود دارد که نشان می دهد از نظر آماری کاهش قابل توجهی در حوادث قلبی عروقی در بیماران مبتلا به دیابت نوع ۲ که تحت درمان با یک مهار کننده SGLT2 (امپاگلیفلوزین ، کاناگلیفلوزین ، داپاگلیفلوزین) یا GLP-1 RA (لیراگلوتید ، سماگلوتید ، دلاگلوتید) قرار داشته اند دیده می شود. افرادي در این مطالعات وارد شدند كه از امپگليفلوزين ، كاناگليفلوزين ، داپاگليفلوزين ، ليراگلوتييد و سماگلوتيد استفاده می کردند و A1C آنها در شروع مطالعه بیش از ۶/۵٪ بوده است و در بیش از ۷۰ درصد از متفورمین به عنوان داروی پایه استفاده می کردند. تعمیم نتایج عملی این مطالعات این است که در بیمارانی که ASCVD اثبات شده دارند و یا ریسک بالای برای ASCVD دارند یکی از این داروها باید در رژیم درمانی دیابت گنجانده شود . برای این بیماران ، استفاده از یکی از مهارکننده های SGLT2 یا GLP-1 RA با اثرات مفید اثبات شده قلبی عروقی توصیه می شود. در مطالعات قلبی عروقی ، امپاگلیفلوزین ، کاناگلیفلوزین ، داپاگلیفلوزین ، لیراگلوتید ، سماگلوتید و دولاگلوتید همه اثرات مفیدی بر شاخص های CKD داشتند .
انسولین درمانی
بسیاری از بیماران مبتلا به دیابت نوع ۲ در نهایت به انسولین درمانی نیاز پیدا می کنند و از آن بهره مند می شوند. برای راهنمایی در مورد نحوه تجویز ایمن و موثر انسولین ، به بخش تزریق انسولین در بالا مراجعه کنید. ماهیت پیشرونده دیابت نوع ۲ باید به طور منظم و عینی برای بیماران توضیح داده شود ، و ارائه دهندگان خدمات باید از استفاده انسولین به عنوان تنبیه یا توصیف آن به عنوان نشانه کوتاهی شخص در مراقبت از خود خودداری کنند. در عوض ، بر سودمندی و اهمیت انسولین برای حفظ کنترل قند خون هنگامی که پیشرفت بیماری بر داروهای خوراکی فائق آمد تاکید شود. آموزش و مشارکت بیماران در مدیریت بیماری خود و استفاده از انسولین حائز اهمیت است. به عنوان مثال ، باید به بیماران آموزش داد تا بتوانند تیتراسیون و تعیین دز متناسب با خود را یاد بگیرند. آموزش جامع در مورد نظارت بر خود بر قند خون ، رژیم غذایی ، و جلوگیری از درمان مناسب قند خون در هر بیمار با استفاده از انسولین بسیار مهم است. همچنین آموزش لازم در مورد نحوه ی آزمایش قند خون، جلو گیری از هیپوگلیسمی و درمان آن در بیمارانی که از انسولین استفاده می کنند اهمیت حیاتی دارد.
انسولین پایه
استفاده از انسولین پایه به تنهایی راحت ترین روش استفاده از انسولین است و می تواند به متفورمین و سایر عوامل خوراکی اضافه شود. دوزهای شروع را می توان بر اساس وزن بدن ( ۰/۱ تا ۰/۲ واحد به ازای هر کیلوگرم وزن بدن در روز) و درجه هیپرگلیسمی تخمین زد و با تیتراسیون طی روزها تا هفته ها به دز متناسب رسید. ماموریت انسولین پایه جلوگیری از تولید گلوکز توسط کبد و محدود کردن قند خون در طول شب و بین وعده های غذایی است. کنترل گلوکز ناشتا را می توان با انسولین NPH انسانی یا انسولین آنالوگ با اثر طولانی به دست آورد. در مطالعات بالینی ، استفاده از آنالوگهای پایه ی طولانی مدت (U-100 glargine یا detemir) در مقایسه با NPH هیپو گلیسمی علامتی و شبانه کمتری ایجاد می کنند. اگر چه این این کاهش ریسک چشمگیر نیست و ممکن است ادامه نداشته باشد. استفاده از آنالوگهای طولانی اثرتر مانند (U-300 glargine یا degludec) در مقایسه با U-100 glargine در ترکیب با داروهای خوراکی احتمال هیپوگلیسمی کمتری دارند. اگر چه کاهش احتمال هیپوگلیسمی به دنبال استفاده از این آنالوگ های طولانی اثر در مقایسه با NPH در مطالعات بالینی به اثبات رسیده است با این وجود این اختلاف ممکن است در دنیای واقعی چشمگیر نباشد. پزشکان باید از احتمال استفاده ی غیر معقول از انسولین پایه ( overbasalisation ) آگاه باشند. علائم استفاده ی زیاد و نابجا از انسولین پایه عبارتند از دز بیش ار ۰/۵ واحد به ازای هر کیلوگرم وزن بدن ، تفاوت زیاد بین قند زمان خواب با قند خون ناشتا ( به عنوان مثال تفاوت بیش از ۵۰ میلی گرم در دسی لیتر بین قند زمان خواب و قند ناشتا) و تفاوت زیاد بین قند قبل و بعد از غذا ، هیپوگلیسمی (آگاه یا ناآگاه) . در صورت وجود موارد بالا باید درمان بیمار مجددا مورد بازنگری قرار گیرد.
هزینه انسولین طی دو دهه گذشته در مقایسه با هزینه های دیگر پزشکی به به طور مداوم در حال افزایش است. این هزینه بار قابل توجهی را به بیماران تحمیل می کند زیرا انسولین برای افرادی که دیابت دارند به یک هزینه در حال رشد تبدیل شده است. این هزینه ها به طور مستقیم منجر به عدم رعایت درمان می شود. بنابراین ، در نظر گرفتن هزینه هایکی از مولفه های مهم مدیریت درمان است. برای بسیاری از بیماران مبتلا به دیابت نوع ۲ (به عنوان مثال ، افرادی با اهداف A1C متوسط، میزان پایین هیپوگلیسمی ، و مقاومت شدید به انسولین ، و همچنین کسانی که از نظر هزینه ای مشکل دارند) ، انسولین انسانی (NPH و رگولار ) ممکن است انتخاب مناسب درمان باشد ، و پزشکان باید با کاربرد آنها آشنا باشند. انسولین رگولار انسانی ، NPH و 70/30 NPH را می توان با قیمت کمتری از داروخانه ها تهیه کرد.
انسولین قبل غذا
بسیاری از افراد مبتلا به دیابت نوع ۲ برای رسیدن به اهداف مناسب قند خون ، علاوه بر انسولین پایه ، به دوز انسولین قبل از غذا نیز نیاز دارند. دوز ۴ واحد یا ۱۰٪ مقدار انسولین پایه در بزرگترین وعده غذایی یا وعده غذایی با بیشترین افزایش قند خون شروع می شود. سپس رژیم انسولین را می توان بر اساس نیاز بیمار تشدید کرد. افراد مبتلا به دیابت نوع ۲ به طور کلی مقاومت بیشتری به انسولین نسبت به افراد مبتلا به دیابت نوع ۱ دارند ، بنابر این به دوزهای روزانه بالاتری ((1 واحد / کیلوگرم) نیاز دارند و به میزان کمتری مبتلا به هیپوگلیسمی می شوند. تیتراسیون می تواند براساس اندازه گیری قند خانگی یا A1C باشد. با افزودنهای قابل توجه به دوز انسولین جمعی ، به ویژه در وعده عصرانه ، باید به کاهش انسولین پایه توجه شود. متاآنالیز مطالعات مقایسه ای استفاده از انسولین سریع اثر آنالوگ با انسولین رگولار انسانی در بیماران دیابتی نوع ۲ تفاوت قابل توجهی در میزان A1C یا میزان بروز هیپوگلیسمی نشان نمی دهند.
انسولین غلیظ
در حال حاضر چندین داروی غلیظ انسولین موجود است. انسولین رگولار U-500 ، طبق تعریف ، پنج برابر غلیظ تر از انسولین رگولار U-100 است. U-500 رگولار دارای فارماکوکینتیک مشخص با شروع تأخیری و مدت زمان طولانی تر نسبت به رگولار U-100 است ، دارای خصوصیاتی بیشتر شبیه انسولین اثر متوسط (NPH) است و می تواند در دو یا سه تزریق روزانه استفاده شود. غلظت U-300 گلارژین و U-200 degludec سه و دو برابر بیشتر از فرمولاسیون های U-100 آنها است و اجازه می دهد دوزهای بالاتر تجویز انسولین پایه در هر حجم واحداستفاده شود. گلارژین U-300 دارای مدت زمان طولانی تری نسبت به U-100 گلارژین است اما نسبت به واحد تجویز اثر متوسط نسبتاً کمتری دارد. FDA همچنین فرمولاسیون غلیظ انسولین سریع اثر لیزپرو ، U-200 (200 واحد در میلی لیتر) و انسولین lispro-aabc (U-200) را تأیید کرده است. تزریقاین داروهای غلیظ ممکن است برای بیماران راحت ترباشد و ممکن است در کسانی که مقاومت به انسولین دارند و به دوزهای زیادی انسولین نیاز دارند ، میزان پایبندی را بهبود ببخشند. در حالی که انسولین معمولی U-500 در هر دو قلم و ویال موجود است ، سایر انسولین های غلیظ فقط در قلم های پر شده در دسترس هستند تا خطر خطاهای دوز را به حداقل برسانند.
انسولین استنشاقی
انسولین استنشاقی به عنوان انسولین سریع اثر در دسترس است. مطالعات انجام شده در افراد مبتلا به دیابت نوع ۱ فارماکوکینتیک سریع را نشان می دهد . دریک مطالعه موردی شواهدی نشان داده شده که در مقایسه با انسولین تزریقی سریع اثر ، دوزهای اضافی انسولین استنشاقی بر اساس میزان قند خون بعد از غذا می تواند باعث بهبود قند خون بدون افزایش خطر هیپوگلیسمی یا افزایش وزن شود ، اگرچه برای تأیید نتایج یک مطالعه بزرگتر لازم است . انسولین استنشاقی در بیماران مبتلا به بیماری مزمن ریوی مانند آسم و بیماری انسدادی مزمن ریوی منع مصرف دارد و در بیمارانی که سیگار می کشند یا اخیراً سیگار را ترک کرده اند توصیه نمی شود. همه بیماران برای شناسایی بیماری بالقوه ریه قبل و بعد از شروع انسولین درمانی استنشاق به اسپیرومتری نیاز دارند.
درمان تزریقی ترکیبی
اگر انسولین پایه به میزان قابل قبول قند خون ناشتا را کاهش داده باشد و یا اگر دوز مصرفی به بیش از ۰/۵ واحد در کیلوگرم در روز رسیده باشد ولی A1C بالاتر از حد هدف باقی مانده باشد، درمان تزریقی ترکیبی را درنظر بگیرید. در این روش می تواند از یک GLP-1 RA اضافه شده به انسولین پایه یا دوزهای مختلف انسولین استفاده کرد.. ترکیبی از انسولین پایه و GLP-1 RA دارای قدرت کاهش دهندگی قوی قند به همراه افزایش وزن کمتر در مقایسه با رژیم های تشدیده شده ی انسولین است. در یک مطالعه دوام بیشتر ثبات قند خون در مقایسه با افزودن انسولین پایه به تنهایی دیده شده است. دو محصول مختلف با ترکیب دوتایی ثابت و مصرف یک بار در روز حاوی انسولین پایه به همراه GLP-1 RA موجود است: انسولین گلارژین به علاوه لیکسیسناتید با نام تجاری سولیکووا(Soliqua) و انسولین دگلودک به اضافه لیراگلوتید با نام تجاری ترسیبا ( Tresiba).
تشدید درمان انسولین را می توان با افزودن دوزهای پراندیال به انسولین پایه انجام داد. شروع با یک تزریق قبل از بزرگترین وعده ی غذای انجام می شود و در صورت لزوم می توان آن را به یک رژیم با پند تزریق قبل از وعده های غذایی افزایش داد ( MDI). در روش دیگر ، در یک بیمار که به دز واحد انسولین پایه جواب مناسب نمی دهد و A1C به هدف نمی رسد می توان از ترکیب انسولین های مخلوط آماده با تزریق دوبار در روز استفاده کرد. هر رویکرد مزایا و معایبی دارد. به عنوان مثال ، رژیم های پایه و بولوس انعطاف پذیری بیشتری برای بیمارانی که برنامه های غذای نامنظمی دارند ارائه می دهند. از طرف دیگر ، دو دوز انسولین مخلوط شده یک وسیله ساده و راحت برای تزریق انسولین در طول روز است. علاوه بر این ، انسولین های انسانی ، به طور جداگانه ، مخلوط شده توسط خود بیمار ، یا به عنوان فرمول های پیش ساخته NPH / رگولار ( ۷۰/۳۰) ، گزینه های کم هزینه تری در مقایسه با ترکیبات آنالوگ هستند. هنگام شروع درمان تزریقی ترکیبی ، درمان با متفورمین باید حفظ شود ، در حالی که سولفونیل اوره و مهار کننده های DPP-4 معمولاً قطع می شوند. در بیماران با کنترل کمتر از حد مطلوب قند خون ، به ویژه در مواردی که به دوزهای انسولین زیادی نیاز دارند ، استفاده اضافی از تیازولیدین دیون یا یک مهار کننده SGLT2 ممکن است به بهبود کنترل و کاهش میزان انسولین مورد نیاز کمک کند ، اگرچه عوارض جانبی بالقوه باید در نظر گرفته شود.

تصویر دوم


